Introducción Bioquímica y el agua
Bioquímica
La definición más acertada es la que expresa que es una rama de la ciencia (fusiona química y biología) encargada de el estudio de las sustancias que se encuentran presentes en los organismos vivos y de las reacciones químicas fundamentales para los procesos vitales.
Las proteínas, los lípidos, los carbohidratos y los ácidos son algunos de los componentes que se analizan desde la bioquímica, disciplina para la cual todo ser viviente posee carbono. Por lo general, se suele indicar que la bioquímica hace foco en el estudio de las bases de la vida, ya que su objeto de estudio son las moléculas que forman parte tanto de células como de tejidos propios de los seres vivos.
Los estudios bioquímicos han permitido avances en el tratamiento de muchas enfermedades metabólicas, y en conocer más sobre el genoma humano. Así como en el campo de la medicina, también se aplica en la odontología, agricultura, práctica forense, antropología, ciencias ambientales, entre otros.
Los elementos importantes encontrados en las células vivas se muestran a color. Los elementos en color rosa (CHNOPS) son los seis elementos más abundantes. Los cinco iones esenciales están en violeta. Los elementos traza se muestran en azul oscuro (más comunes) y en azul claro (los menos comunes).
En el estudio de las reacciones químicas, una de las especialidades de la bioquímica se encuentra en el análisis de los nutrientes, los cuales se dividen en cinco grupos específicos: proteínas, grasas, hidratos de carbono, vitaminas y minerales; en ellos se incluyen 50 sustancias que según parece son indispensables para conseguir una salud equilibrada y un crecimiento normal. Nuestro organismo requiere de la energía para poder realizar cualquier actividad, incluso para efectuar el mero mecanismo de respirar. Gracias a la invención del calorímetro, los investigadores pueden conocer cuáles son los nutrientes que aportan la cantidad de energía que un organismo necesita; cabe mencionar que de acuerdo a la actividad que se realice las demandas energéticas difieren. El estudio de los bioquímicos consiste en saber cuánta energía aporta cada uno de estos nutrientes y gracias a ello es posible saber que 1 gramo de proteína o de hidrato de carbono puro produce 4 calorías mientras que 1 gr de grasa pura produce 9. Cabe aclarar que cada nutriente cumple con una función particular:
* Las proteínas son las encargadas de producir tejido corporal y de sintetizar las enzimas, y la cantidad de proteína recomendada para una persona adulta es de 0,8 gramos por kilo de peso;
* Los minerales se encargan de la reconstrucción estructural de los tejidos corporales y colaboran con la acción de los sistemas enzimáticos (contracción muscular, reacciones nerviosas y coagulación de la sangre). Los minerales fundamentales son el calcio, el fósforo, el magnesio, el hierro, el sodio y el potasio;
* Las vitaminas son las que ayudan a mejorar la forma de absorción de las proteínas, los hidratos de carbono y las grasas. Existen muchos tipos de vitaminas, siendo las más importantes aquéllas que participan en la formación de las células de la sangre, de las hormonas y del hígado;
* Los hidratos de carbono son los principales nutrientes para el aporte de energía ya que se encuentran en la mayor cantidad de alimentos, así como también en bebidas alcohólicas. Durante el proceso de metabolismo los hidratos de carbono se queman con el fin de obtener energía;
* Las grasas aportan al organismo más del 50% de la energía, y son un combustible de tipo compacto que se almacena perfectamente para ser utilizado cuando sea necesario. Si bien en un ambiente natural son nutrientes indispensables (permiten crear reservas durante los períodos de comida abundante para consumir al momento de la escasez), en nuestras sociedades modernas donde siempre hay alimentos a nuestras disposición, se han convertido en una causa fundamental de los problemas de salud.
La célula
Es la unidad básica de la vida
A. Célula Procariota
En el estudio de las reacciones químicas, una de las especialidades de la bioquímica se encuentra en el análisis de los nutrientes, los cuales se dividen en cinco grupos específicos: proteínas, grasas, hidratos de carbono, vitaminas y minerales; en ellos se incluyen 50 sustancias que según parece son indispensables para conseguir una salud equilibrada y un crecimiento normal. Nuestro organismo requiere de la energía para poder realizar cualquier actividad, incluso para efectuar el mero mecanismo de respirar. Gracias a la invención del calorímetro, los investigadores pueden conocer cuáles son los nutrientes que aportan la cantidad de energía que un organismo necesita; cabe mencionar que de acuerdo a la actividad que se realice las demandas energéticas difieren. El estudio de los bioquímicos consiste en saber cuánta energía aporta cada uno de estos nutrientes y gracias a ello es posible saber que 1 gramo de proteína o de hidrato de carbono puro produce 4 calorías mientras que 1 gr de grasa pura produce 9. Cabe aclarar que cada nutriente cumple con una función particular:
* Las proteínas son las encargadas de producir tejido corporal y de sintetizar las enzimas, y la cantidad de proteína recomendada para una persona adulta es de 0,8 gramos por kilo de peso;
* Los minerales se encargan de la reconstrucción estructural de los tejidos corporales y colaboran con la acción de los sistemas enzimáticos (contracción muscular, reacciones nerviosas y coagulación de la sangre). Los minerales fundamentales son el calcio, el fósforo, el magnesio, el hierro, el sodio y el potasio;
* Las vitaminas son las que ayudan a mejorar la forma de absorción de las proteínas, los hidratos de carbono y las grasas. Existen muchos tipos de vitaminas, siendo las más importantes aquéllas que participan en la formación de las células de la sangre, de las hormonas y del hígado;
* Los hidratos de carbono son los principales nutrientes para el aporte de energía ya que se encuentran en la mayor cantidad de alimentos, así como también en bebidas alcohólicas. Durante el proceso de metabolismo los hidratos de carbono se queman con el fin de obtener energía;
* Las grasas aportan al organismo más del 50% de la energía, y son un combustible de tipo compacto que se almacena perfectamente para ser utilizado cuando sea necesario. Si bien en un ambiente natural son nutrientes indispensables (permiten crear reservas durante los períodos de comida abundante para consumir al momento de la escasez), en nuestras sociedades modernas donde siempre hay alimentos a nuestras disposición, se han convertido en una causa fundamental de los problemas de salud.
La célula
Importancia del agua
El agua es el líquido más abundante de la corteza y uno de los pocos líquidos naturales. Es esencial en los seres vivos. El agua es el componente más abundante en los medios orgánicos, los seres vivos contienen por término medio un 70% de agua.
En el agua viven gran cantidad de animales y plantas. En los mares, ríos, lagos, lagunas, existen buenas condiciones para encontrar alimentos y poder vivir. Los animales acuáticos pueden comer plantas y otros animales pequeños que viven en el agua. Animales y plantas microscópicos forman un conjunto de sustancias nutritivas, llamado Plancton, que es la fuente de alimentos para peces, aves, larvas y mamíferos acuáticos de mayos tamaño.
El agua es un tesoro valioso de nuestro planeta. Gracias a ellas viven los animales, las plantas y nosotros mismos. Cuando falta el agua, todos sufrimos las consecuencias: las plantas y los animales mueren, algunos alimentos escasean en el mercado y en nuestras casas no podemos disponer de toda el agua necesaria.
En el agua viven gran cantidad de animales y plantas. En los mares, ríos, lagos, lagunas, existen buenas condiciones para encontrar alimentos y poder vivir. Los animales acuáticos pueden comer plantas y otros animales pequeños que viven en el agua. Animales y plantas microscópicos forman un conjunto de sustancias nutritivas, llamado Plancton, que es la fuente de alimentos para peces, aves, larvas y mamíferos acuáticos de mayos tamaño.
El agua es un tesoro valioso de nuestro planeta. Gracias a ellas viven los animales, las plantas y nosotros mismos. Cuando falta el agua, todos sufrimos las consecuencias: las plantas y los animales mueren, algunos alimentos escasean en el mercado y en nuestras casas no podemos disponer de toda el agua necesaria.
Aminoacidos , peptidos y proteinas
AMINOÁCIDOS
AMINOÁCIDOS
¿Qué son?
Los aminoácidos son sustancias orgánicas que contiene al menos un grupo amino (-NH2) y al menos un grupo ácido, que siempre es el grupo carboxilo (-COOH) excepto en el caso de la taurina (que es -SO3H). De esta manera se puede establecer una fórmula estructural general para todos los aminoácidos, que es la que podemos ver en la figura. En ella R es la cadena lateral que es distintiva para cada aminoácido.
 Características generales
Es importante destacar que el carbono marcado como α en la figura es un carbono asimétrico (está unido a cuatro radicales diferentes) en todos los aminoácidos con excepción de la glicina. Esto significa que todos los aminoácidos tiene actividad óptica (cuando están en una solución desvían el plano de la luz polarizada hacia la izquierda o hacia la derecha), menos la glicina. Solo los aminoácidos levógiros, L, forman parte de las proteínas.
Otra característica importante de los aminoácidos es que son anfóteros. Esto quiere decir que cuando están disueltos en agua acuosa, los aminoácidos son capaces de ionizarse como un ácido cuando el pH es básico, como una base cuando el pH es ácido o como un ácido y una base a la vez cuando el pH es neutro.
Características generales
Es importante destacar que el carbono marcado como α en la figura es un carbono asimétrico (está unido a cuatro radicales diferentes) en todos los aminoácidos con excepción de la glicina. Esto significa que todos los aminoácidos tiene actividad óptica (cuando están en una solución desvían el plano de la luz polarizada hacia la izquierda o hacia la derecha), menos la glicina. Solo los aminoácidos levógiros, L, forman parte de las proteínas.
Otra característica importante de los aminoácidos es que son anfóteros. Esto quiere decir que cuando están disueltos en agua acuosa, los aminoácidos son capaces de ionizarse como un ácido cuando el pH es básico, como una base cuando el pH es ácido o como un ácido y una base a la vez cuando el pH es neutro.
 Clasificación de los aminoácidos
En la naturaleza existen numerosos aminoácidos diferentes, pero sólo unos 20 forman parte de las proteínas, son los que llamamos proteinogénicos. Aquí solo nos ocuparemos de estos 20 aminoácidos.
Clasificación de los aminoácidos
En la naturaleza existen numerosos aminoácidos diferentes, pero sólo unos 20 forman parte de las proteínas, son los que llamamos proteinogénicos. Aquí solo nos ocuparemos de estos 20 aminoácidos.
Por otra parte, algunos de los aminoácidos no son sintetizables por el organismo y, por tanto, tienen que ser suministrados con la dieta. A estos se les llama aminoácidosesenciales. Para la especie humana existen ocho aminoácidos esenciales: treonina, metionina, lisina, valina, triptófano, leucina, isoleucina y fenilalanina. La histidina se considera como esencial durante el crecimiento, pero no así en el adulto.

¿Qué son?
Los aminoácidos son sustancias orgánicas que contiene al menos un grupo amino (-NH2) y al menos un grupo ácido, que siempre es el grupo carboxilo (-COOH) excepto en el caso de la taurina (que es -SO3H). De esta manera se puede establecer una fórmula estructural general para todos los aminoácidos, que es la que podemos ver en la figura. En ella R es la cadena lateral que es distintiva para cada aminoácido.
Es importante destacar que el carbono marcado como α en la figura es un carbono asimétrico (está unido a cuatro radicales diferentes) en todos los aminoácidos con excepción de la glicina. Esto significa que todos los aminoácidos tiene actividad óptica (cuando están en una solución desvían el plano de la luz polarizada hacia la izquierda o hacia la derecha), menos la glicina. Solo los aminoácidos levógiros, L, forman parte de las proteínas.
Otra característica importante de los aminoácidos es que son anfóteros. Esto quiere decir que cuando están disueltos en agua acuosa, los aminoácidos son capaces de ionizarse como un ácido cuando el pH es básico, como una base cuando el pH es ácido o como un ácido y una base a la vez cuando el pH es neutro.
Clasificación de los aminoácidos
En la naturaleza existen numerosos aminoácidos diferentes, pero sólo unos 20 forman parte de las proteínas, son los que llamamos proteinogénicos. Aquí solo nos ocuparemos de estos 20 aminoácidos.
Por otra parte, algunos de los aminoácidos no son sintetizables por el organismo y, por tanto, tienen que ser suministrados con la dieta. A estos se les llama aminoácidosesenciales. Para la especie humana existen ocho aminoácidos esenciales: treonina, metionina, lisina, valina, triptófano, leucina, isoleucina y fenilalanina. La histidina se considera como esencial durante el crecimiento, pero no así en el adulto.

Por otra parte, algunos de los aminoácidos no son sintetizables por el organismo y, por tanto, tienen que ser suministrados con la dieta. A estos se les llama aminoácidosesenciales. Para la especie humana existen ocho aminoácidos esenciales: treonina, metionina, lisina, valina, triptófano, leucina, isoleucina y fenilalanina. La histidina se considera como esencial durante el crecimiento, pero no así en el adulto.
PÉPTIDOS
¿Qué son?
Un péptido es una molécula que resulta de la unión de dos o más aminoácidos (AA) mediante enlaces amida. En los péptidos y en las proteínas, estos enlaces amida reciben el nombre de enlaces peptídicos y son el resultado de la reacción del grupo carboxilo de un AA con el grupo amino de otro, con eliminación de una molécula de agua. Generalmente se considera, según el autor, que los péptidos no son mayores de 50 o 100 aminoácidos. De manera también general a una cadena polipeptídica se le considera péptido y no proteína si su peso molecular es menor de 5.000 daltons.
Tipos de péptidos
Cuando el péptido está formado por menos de 10 AA se trata de un oligopéptido (dipéptido, tripéptido, etc.). Cuando contiene entre 10 y 50 AA se trata de un polipéptido y si el número de AA es mayor, se habla de proteínas. En los seres vivos se pueden encontrar proteínas formadas por más de 1000 AA.
Independientemente de la longitud de la cadena polipeptídica, siempre habrá un grupo NH2 que no ha reaccionado (el extremo amino) y un grupo COOH que tampoco ha reaccionado (el extremo carboxilo). Cada péptido o polipéptido se suele escribir, convencionalmente, de izquierda a derecha, empezando por el extremo N-terminal que posee un grupo amino libre y finalizando por el extremo C-terminal en el que se encuentra un grupo carboxilo libre. A la hora de nombrar un oligopéptido se considera como AA principal al que conserva el grupo carboxilo. El resto de los AA se nombran como sustituyentes, comenzando por el AA que ocupa el extremo amino. Así, por ejemplo, un tripéptido Pro-Tyr-Lys se denominará prolil-tirosil-lisina.
Funciones
Entre las diversas funciones naturales que pueden desarrollar los péptidos podemos destacar:
1. Agentes vasoactivos. Regulan la presión arterial. Un ejemplo es la angiotensina II, un octapéptido que se origina mediante la hidrólisis de una proteína precursora que se llama angiotensinógeno, y que no tiene actividad vasopresora. Otro ejemplo sería la bradiquinina, un nonapéptido hipotensor (actividad vasodilatadora).
2. Hormonas. Aquí tenemos numerosos ejemplos. Los más importantes:
- Oxitocina: nonapéptido segregado por la hipófisis. Provoca la contracción uterina y la secreción de leche por la glándula mamaria, facilitando el parto y la alimentación del recién nacido.
- Vasopresina: nonapéptido que aumenta la reabsorción de agua en el riñón (hormona antidiurética).
- Somatostatina: 14 aminoácidos. Inhibe la liberación de la hormona del crecimiento
- Insulina: 51 aminoácidos. Estimula la absorción de glucosa por parte de las células (disminuye la presencia de glucosa en sangre). Fue el primer péptido que se secuenció por métodos químicos.
- Glucagón: 29 aminoácidos. Sus efectos son los contrarios a los de la insulina, ayuda a aumentar los niveles de glucosa en sangre.
3. Neurotransmisores. Entre los péptidos que realizan estas funciones tenemos las encefalinas (5 AAs), la β-endorfina (31 AAs) y la sustancia P (11 AAs).
Antioxidantes. El papel del tripéptido glutation es esencial como antioxidante celular. Reduce las especies reactivas del oxígeno, tóxicas para la célula.
Un péptido es una molécula que resulta de la unión de dos o más aminoácidos (AA) mediante enlaces amida. En los péptidos y en las proteínas, estos enlaces amida reciben el nombre de enlaces peptídicos y son el resultado de la reacción del grupo carboxilo de un AA con el grupo amino de otro, con eliminación de una molécula de agua. Generalmente se considera, según el autor, que los péptidos no son mayores de 50 o 100 aminoácidos. De manera también general a una cadena polipeptídica se le considera péptido y no proteína si su peso molecular es menor de 5.000 daltons.
Tipos de péptidos
Cuando el péptido está formado por menos de 10 AA se trata de un oligopéptido (dipéptido, tripéptido, etc.). Cuando contiene entre 10 y 50 AA se trata de un polipéptido y si el número de AA es mayor, se habla de proteínas. En los seres vivos se pueden encontrar proteínas formadas por más de 1000 AA.
Independientemente de la longitud de la cadena polipeptídica, siempre habrá un grupo NH2 que no ha reaccionado (el extremo amino) y un grupo COOH que tampoco ha reaccionado (el extremo carboxilo). Cada péptido o polipéptido se suele escribir, convencionalmente, de izquierda a derecha, empezando por el extremo N-terminal que posee un grupo amino libre y finalizando por el extremo C-terminal en el que se encuentra un grupo carboxilo libre. A la hora de nombrar un oligopéptido se considera como AA principal al que conserva el grupo carboxilo. El resto de los AA se nombran como sustituyentes, comenzando por el AA que ocupa el extremo amino. Así, por ejemplo, un tripéptido Pro-Tyr-Lys se denominará prolil-tirosil-lisina.
Funciones
Entre las diversas funciones naturales que pueden desarrollar los péptidos podemos destacar:
1. Agentes vasoactivos. Regulan la presión arterial. Un ejemplo es la angiotensina II, un octapéptido que se origina mediante la hidrólisis de una proteína precursora que se llama angiotensinógeno, y que no tiene actividad vasopresora. Otro ejemplo sería la bradiquinina, un nonapéptido hipotensor (actividad vasodilatadora).
2. Hormonas. Aquí tenemos numerosos ejemplos. Los más importantes:
- Oxitocina: nonapéptido segregado por la hipófisis. Provoca la contracción uterina y la secreción de leche por la glándula mamaria, facilitando el parto y la alimentación del recién nacido.
- Vasopresina: nonapéptido que aumenta la reabsorción de agua en el riñón (hormona antidiurética).
- Somatostatina: 14 aminoácidos. Inhibe la liberación de la hormona del crecimiento
- Insulina: 51 aminoácidos. Estimula la absorción de glucosa por parte de las células (disminuye la presencia de glucosa en sangre). Fue el primer péptido que se secuenció por métodos químicos.
- Glucagón: 29 aminoácidos. Sus efectos son los contrarios a los de la insulina, ayuda a aumentar los niveles de glucosa en sangre.
3. Neurotransmisores. Entre los péptidos que realizan estas funciones tenemos las encefalinas (5 AAs), la β-endorfina (31 AAs) y la sustancia P (11 AAs).
Antioxidantes. El papel del tripéptido glutation es esencial como antioxidante celular. Reduce las especies reactivas del oxígeno, tóxicas para la célula.
PROTEÍNAS
Las proteínas con biomoléculas de alto peso molecular constituidas por una cadena lineal de aminoácidos unidos por enlaces peptídicos que se mantiene plegada de forma que muestra una estructura tridimensional.
Las proteínas desempeñan numerosas funciones en el organismo. De manera muy genérica, según su función, se clasifican como proteínas estructurales o proteínas con actividad biológica.
- Las proteínas estructurales son aquellas que intervienen en la constitución de los tejidos, órganos y células. Como ejemplos se puede citar al colágeno, que forma parte de la piel, ligamentos, tendones, hueso y matriz de varios órganos.
- Las proteínas con actividad biológica son aquellas que intervienen o facilitan un proceso bioquímico en el organismo. Las funciones aquí son casi innumerables, desde regulación de procesos metabólicos hasta participación en la defensa (sistema inmune), pasando por ser moléculas de transporte de otras moléculas en la sangre, por ejemplo.

Molécula de hemoglobina
De acuerdo con la composición química las proteínas, se clasifican en dos tipos principales:
- Simples. Constituidas únicamente aminoácidos. Entre ellas tenemos albúminas, globulinas, histonas…
- Conjugadas. Tienen en su composición otras moléculas diferentes además de los aminoácidos. A esa parte no aminoacídica se le denomina grupo prostético. Entre ellas tenemos las glucoproteínas o mucoproteínas, lipoproteínas, metaloproteínas…
Hablar de las proteínas nos podría llevar varios posts solo para definir todas sus funciones o tipos, así que, por ahora, vamos a dejarlo aquí, quedándonos con la idea de que las proteínas son las moléculas que ejecutan la mayor parte de las tareas de los organismos.

Las proteínas con biomoléculas de alto peso molecular constituidas por una cadena lineal de aminoácidos unidos por enlaces peptídicos que se mantiene plegada de forma que muestra una estructura tridimensional.
Las proteínas desempeñan numerosas funciones en el organismo. De manera muy genérica, según su función, se clasifican como proteínas estructurales o proteínas con actividad biológica.
- Las proteínas estructurales son aquellas que intervienen en la constitución de los tejidos, órganos y células. Como ejemplos se puede citar al colágeno, que forma parte de la piel, ligamentos, tendones, hueso y matriz de varios órganos.
- Las proteínas con actividad biológica son aquellas que intervienen o facilitan un proceso bioquímico en el organismo. Las funciones aquí son casi innumerables, desde regulación de procesos metabólicos hasta participación en la defensa (sistema inmune), pasando por ser moléculas de transporte de otras moléculas en la sangre, por ejemplo.
Molécula de hemoglobina
De acuerdo con la composición química las proteínas, se clasifican en dos tipos principales:
- Simples. Constituidas únicamente aminoácidos. Entre ellas tenemos albúminas, globulinas, histonas…
- Conjugadas. Tienen en su composición otras moléculas diferentes además de los aminoácidos. A esa parte no aminoacídica se le denomina grupo prostético. Entre ellas tenemos las glucoproteínas o mucoproteínas, lipoproteínas, metaloproteínas…
Hablar de las proteínas nos podría llevar varios posts solo para definir todas sus funciones o tipos, así que, por ahora, vamos a dejarlo aquí, quedándonos con la idea de que las proteínas son las moléculas que ejecutan la mayor parte de las tareas de los organismos.

Enzimas
Enzimas
 Los enzimas son proteínas que catalizan reacciones químicas en los seres vivos.
Los enzimas son proteínas que catalizan reacciones químicas en los seres vivos.
Aspectos generales de las enzimas:
Los enzimas, a diferencia de los catalizadores inorgánicos catalizan reacciones específicas. Sin embargo hay distintos grados de especificidad. El enzima sacarasa es muy específico: rompe el enlace b-glucosídico de la sacarosa o de compuestos muy similares.

Carbohidratos
Clasificación Característica
Monosacáridos Unidad más pequeña de estructura delos carbohidratos.
Oligosacáridos Son polímeros con 2 hasta 10 residuos demonosacáridos.
Polisacáridos Son polímeros que contienen muchos (en general más de 20) residuos de monosacáridos.
Glucoconjugados Son derivados de carbohidratos en los que una o máscadenas de carbohidratos están unidas enforma covalente a un péptido, proteína o unlípido.
¿Qué son los carbohidratos? Los carbohidratos, también llamados glúcidos, carbohidratos, hidratos de carbono o sacáridos, son elementos principales en la alimentación, que se encuentran principalmente en azúcares, almidones y fibra. La función principal de los carbohidratos es el aporte energético. Son una de las sustancias principales que necesita nuestro organismo,junto a las grasas y las proteínas.
 Carbohidratos en los alimentos
Los carbohidratos se encuentran en una amplia variedad de alimentos entre los que se encuentras el pan, alubias, leche, palomitas de maíz, patatas, galletas, fideos, gaseosas, maíz o pastel de cereza. También vienen en una variedad de formas.
Las formas más comunes y abundantes son los azúcares, fibras y almidones.
Carbohidratos en los alimentos
Los carbohidratos se encuentran en una amplia variedad de alimentos entre los que se encuentras el pan, alubias, leche, palomitas de maíz, patatas, galletas, fideos, gaseosas, maíz o pastel de cereza. También vienen en una variedad de formas.
Las formas más comunes y abundantes son los azúcares, fibras y almidones.
Tipos de carbohidratos
 Los carbohidratos o hidratos de carbono se agrupan en dos categorías principales.
Los carbohidratos o hidratos de carbono se agrupan en dos categorías principales.
Funciones de los carbohidratos
 Los glúcidos cumplen un papel muy importante en nuestro organismo, que incluyen
Los glúcidos cumplen un papel muy importante en nuestro organismo, que incluyen
 Energía – Los carbohidratos aportan 4 kilocalorías (KCal) por gramo de peso neto, sin agua.
Una vez repuestas y cubiertas todas las necesidades de energía del cuerpo, una pequeña parte se almacena en el hígado y los músculos en forma de glucógeno (normalmente no más de 0,5% del peso de la persona), el resto se transforma en tejido adiposo y se almacena en el organismo como grasas.
Se suele recomendar que minimamente se efectúe una ingesta diaria de 100 gramos de hidratos de carbono para mantener los procesos metabólicos.
Ahorro de proteínas – Cuando el cuerpo no dispone de suficientes hidratos de carbono, éste utilizará las proteínas con fines energéticos, consumiéndolas e impidiéndolas, por tanto, realizar otras funciones de construcción.
Energía – Los carbohidratos aportan 4 kilocalorías (KCal) por gramo de peso neto, sin agua.
Una vez repuestas y cubiertas todas las necesidades de energía del cuerpo, una pequeña parte se almacena en el hígado y los músculos en forma de glucógeno (normalmente no más de 0,5% del peso de la persona), el resto se transforma en tejido adiposo y se almacena en el organismo como grasas.
Se suele recomendar que minimamente se efectúe una ingesta diaria de 100 gramos de hidratos de carbono para mantener los procesos metabólicos.
Ahorro de proteínas – Cuando el cuerpo no dispone de suficientes hidratos de carbono, éste utilizará las proteínas con fines energéticos, consumiéndolas e impidiéndolas, por tanto, realizar otras funciones de construcción.
Los enzimas son catalizadores, es decir, sustancias que, sin consumirse en una reacción, aumentan notablemente su velocidad. No hacen factibles las reacciones imposibles, sino que sólamente aceleran las que espontáneamente podrían producirse. Ello hace posible que en condiciones fisiológicas tengan lugar reacciones que sin catalizador requerirían condicione extremas de presión, temperatura o pH.
Carbohidratos
Clasificación Característica
|
Monosacáridos Unidad más pequeña de estructura delos carbohidratos.
|
Oligosacáridos Son polímeros con 2 hasta 10 residuos demonosacáridos.
|
Polisacáridos Son polímeros que contienen muchos (en general más de 20) residuos de monosacáridos.
· Homoglicano
· Heteroglicano
|
Glucoconjugados Son derivados de carbohidratos en los que una o máscadenas de carbohidratos están unidas enforma covalente a un péptido, proteína o unlípido.
· Proteoglicanos
· Peptidoglicanos
· Glucoproteinas
· Glucolipidos
|

 Energía – Los carbohidratos aportan 4 kilocalorías (KCal) por gramo de peso neto, sin agua.
Energía – Los carbohidratos aportan 4 kilocalorías (KCal) por gramo de peso neto, sin agua.
Lípidos Los lípidos son biomoléculas orgánicas formadas
básicamente por carbono e hidrógeno y generalmente, en menor
proporción, también oxígeno. Además ocasionalmente pueden contener también
fósforo, nitrógeno y azufre .
Los lípidos son biomoléculas orgánicas formadas
básicamente por carbono e hidrógeno y generalmente, en menor
proporción, también oxígeno. Además ocasionalmente pueden contener también
fósforo, nitrógeno y azufre .
 Ácidos grasos
Ácidos grasos
Los ácidos grasos son los componentes
característicos de muchos lípidos y rara vez se
Los lípidos también pueden clasificarse según su
consistencia a temperatura ambiente:
Dentro del grupo de las grasas, mención aparte
merecen las margarinas. Este alimento
Lípidos
Nombre
|
Número
de carbonos
|
Ácido palmítico
|
16 saturado
|
Ácido esteárico
|
18 saturado
|
Ácido oleico
|
18 insaturado
|
18 insaturado
|
|
Ácido linolénico
|
18 insaturado
|
Ácido araquidónico
|
20 insaturado
|
Los tres últimos, que constituyen la vitamina F, no
son sintetizables por el hombre, por lo que
debe incluirlos en su dieta.
Grasas

Una de las reacciones características de los ácidos
grasos es la llamada reacción de
esterificación mediante la cual un ácido graso se une a un alcohol mediante
un enlace covalente,
formando un éster y liberándose una molécula de agua
como se ilustra en la figura.
En los alimentos que normalmente consumimos siempre
nos encontramos con una
combinación de ácidos grasos saturados e
insaturados. Los ácidos grasos saturados son
más difíciles
de utilizar por el organismo, ya que sus posibilidades de combinarse con otras
moléculas están limitadas por estar todos sus posibles puntos de enlace ya
utilizados o "saturados". Esta dificultad para combinarse con otros compuestos
hace que sea difícil romper sus moléculas en otras más pequeñas que atraviesen
las paredes de los capilares sanguíneos y las membranas celulares. Por eso, en
determinadas condiciones pueden acumularse y formar placas en el interior de
las arterias (arteriosclerosis).
Dependiendo del tipo de ácido graso mayoritario las
grasas pueden ser de tres tipos:
Monoinsaturadas (con presencia mayoritaria de ácidos
grasos monoinsaturados) abundante en: aceite de oliva y frutos secos
Poliinsaturadas (con presencia mayoritaria de ácidos
grasos poliinsaturados) abundante en: aceite de girasol y pescados azules
Saturadas (con presencia mayoritaria de ácidos
grasos saturados) abundante en: grasas animales y aceite de palma
FOSFOGLICÉRIDOS O FOSFOLÍPIDOS.
Siguiendo en importancia nutricional se encuentran
los fosfolípidos, que incluyen
fósforo en sus moléculas. Entre otras cosas, forman
las membranas de nuestras células
y actúan como detergentes biológicos.
ESTEROIDES

Son derivados
del anillo del ciclopentanoperhidrofenantreno. A estos compuestos se los conoce
con el nombre de esteroides. En este grupo destaca el colesterol, que es el compuesto
causante de la arteriosclerosis. El colesterol cuya fórmula se muestra en la figura
consta del ciclopentanoperhidrofenantreno con un grupo –OH en el carbono 3 y
una cadena hidrocarbonada en el carbono 17.
FUNCIONES DE
LOS LÍPIDOS.
Los lípidos desempeñan cuatro tipos de funciones
Función de reserva. Son la principal reserva
energética del organismo. Un gramo de grasa produce 9'4 kilocalorías en las
reacciones metabólicas de oxidación, mientras que proteínas y glúcidos sólo
producen 4'1 kilocaloría/gr.
Función estructural. Forman las bicapas lipídicas de
las membranas. Recubren órganos y le dan consistencia, o protegen mecánicamente
como el tejido adiposo de pies y manos.
Función biocatalizadora. En este papel los lípidos
favorecen o facilitan las reacciones químicas que se producen en los seres
vivos.
Función transportadora. El transporte de lípidos
desde el intestino hasta su lugar de destino
se realiza mediante su emulsión gracias a los ácidos biliares y a los
proteolípidos, asociaciones de proteínasespecíficas con triacilglicéridos,
colesterol, fosfolípidos, etc., que permiten su transporte por sangre y linfa.
ACIDOS
NUCLEICOS
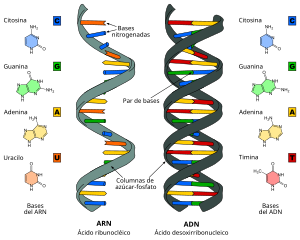

Son compuestos orgánicos de elevado peso molecular,
formados por carbono, hidrógeno, oxígeno, nitrógeno y fósforo. Cumplen la
importante función de sintetizar las proteínas específicas de las células y de
almacenar, duplicar y transmitir los caracteres hereditarios. Los ácidos
nucleicos, representados por el ADN (ácido desoxirribonucleico) y por el ARN
(ácido ribonucleico), son macromoléculas formadas por la unión de moléculas más
pequeñas llamadasnucleótidos.
NUCLEÓTIDOS
Son moléculas compuestas por grupos fosfato, un
monosacárido de cinco carbonos (pentosa) y una base nitrogenada. Además de
constituir los ácidos nucleicos forman parte de coenzimas y de moléculas que
contienen energía. Los nucleótidos tienen importantes funciones, entre ellas el
transporte de átomos en la cadena respiratoria mitocondrial, intervenir en el
proceso de fotosíntesis, transporte de energía principalmente en forma de
adenosin trifosfato (ATP) y transmisión de los caracteres hereditarios.
Esquema de un nucleótido
Grupos
fosfato
Son los que dan la característica ácida al ADN y
ARN. Estos ácidos nucleicos, al tener nucleótidos con un solo radical
(monofosfato) son estables. Cuando el nucleótido contiene más grupos fosfato
(difosfato, trifosfato) se vuelve inestable, como sucede con el adenosin
trifosfato o ATP. En consecuencia, se rompe un enlace fosfato y se libera la
energía que lo une al nucleótido. Los grupos fosfato forman parte de la bicapa
lipídica de las membranas celulares.
Pentosas
Son monosacáridos con cinco carbono en su molécula.
En los ácidos nucleicos hay dos tipos de pentosas, la desoxirribosa presente en
el ADN y la ribosa, que forma parte del ARN.
Bases nitrogenadas
También hay dos tipos. Las derivadas de la purina
son la adenina y la guanina y las que derivan de la pirimidina son la citosina,
la timina y el uracilo.
Bases nitrogenadas
La timina está presente solo en el ADN, mientras que
el uracilo está únicamente en el ARN. El resto de las bases nitrogenadas forma
parte de ambos ácidos nucleicos.
La asociación de los nucleótidos con otras
estructuras moleculares permite la transmisión de caracteres hereditarios y el
transporte de energía.
NUCLEÓSIDOS
Es la unión de una pentosa con una base nitrogenada,
a través del carbono 1’ del monosacárido con un nitrógeno de la base. Al
establecerse la unión química se desprende una molécula de agua.
Esquema de un nucleósido
Los nucleósidos se identifican de acuerdo a la base
nitrogenada de la cual provienen. Si derivan de bases purínicas llevan el
sufijo “osina”. Si lo hacen de bases pirimidínicas se agrega la terminación
“idina”. Además, si el nucleósido está unido a la desoxirribosa se le agrega el
prefijo “desoxi”.
Nomenclatura de los nucleósidos
De acuerdo a lo señalado, un nucleótido está formado
por un nucleósido unido a uno o más grupos fosfato. Los nucleótidos se
identifican de manera similar que los nucleósidos, omitiendo la última vocal y
añadiendo la palabra “fosfato”, por ejemplo, adenosin fosfato, desoxicitidin
fosfato, uridin fosfato, etc.
Los ácidos nucleicos son larguísimas cadenas
formadas por millones de nucleótidos que se unen entre sí por enlaces de
fosfatos. La base nitrogenada del nucleótido se une al carbono 1’ de la
molécula de pentosa y el grupo fosfato al carbono 5’. La columna vertebral de
la cadena o hilera la constituyen el grupo fosfato y la pentosa.
ACIDO
DESOXIRRIBONUCLEICO (ADN)
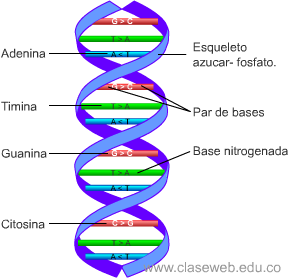

 Ácido desoxirribonucleico (ADN), material genético de todos los organismos celulares y casi todos los virus. El ADN lleva la información necesaria para dirigir la síntesis de proteínas y la replicación. Se llama síntesis de proteínas a la producción de lasproteínas que necesita la célula o el virus para realizar sus actividades y desarrollarse.
Ácido desoxirribonucleico (ADN), material genético de todos los organismos celulares y casi todos los virus. El ADN lleva la información necesaria para dirigir la síntesis de proteínas y la replicación. Se llama síntesis de proteínas a la producción de lasproteínas que necesita la célula o el virus para realizar sus actividades y desarrollarse. La replicación es el conjunto de reacciones por medio de las cuales el
La replicación es el conjunto de reacciones por medio de las cuales el 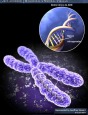 ADN se copia a sí mismo cada vez que una célula o un virus se reproduce y transmite a la descendencia la información que contiene.En casi todos los organismos celulares el ADN está organizado en forma de cromosomas, situados en el núcleo de la célula.
ADN se copia a sí mismo cada vez que una célula o un virus se reproduce y transmite a la descendencia la información que contiene.En casi todos los organismos celulares el ADN está organizado en forma de cromosomas, situados en el núcleo de la célula.
Estructura del ADN
 Cada molécula de ADN está constituida por dos cadenas o bandas formadas por un elevado número de compuestos químicos llamados nucleótidos.
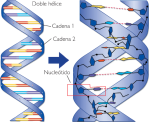
Cada molécula de ADN está constituida por dos cadenas o bandas formadas por un elevado número de compuestos químicos llamados nucleótidos.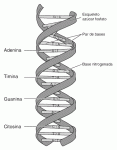 Estas cadenas forman una especie de escalera retorcida que se llama doble hélice. Cada nucleótido está formado por tres unidades: una molécula de azúcar llamada desoxirribosa, un grupo fosfato y uno de cuatro posibles compuestos nitrogenados llamados bases: adenina (abreviada como A), guanina (G), timina (T) y citosina (C).
Estas cadenas forman una especie de escalera retorcida que se llama doble hélice. Cada nucleótido está formado por tres unidades: una molécula de azúcar llamada desoxirribosa, un grupo fosfato y uno de cuatro posibles compuestos nitrogenados llamados bases: adenina (abreviada como A), guanina (G), timina (T) y citosina (C).
La molécula de desoxirribosa ocupa el centro del nucleótido y está flanqueada por un grupo fosfato a un lado y una base al otro. El grupo fosfato está a su vez unido a la desoxirribosa del nucleótido adyacente de la cadena. Estas subunidades enlazadas desoxirribosa-fosfato forman los lados de la escalera; las bases están enfrentadas por parejas, mirando hacia el interior, y forman los travesaños.
Los nucleótidos de cada una de las dos cadenas que forman el ADN establecen una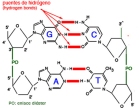 asociación específica con los correspondientes de la otra cadena. Debido a la afinidad química entre las bases, los nucleótidos que contienen adenina se acoplan siempre con los que contienen timina, y los que contienen citosina con los que contienen guanina. Las bases complementarias se unen entre sí por enlaces químicos débiles llamados enlaces de hidrógeno.
asociación específica con los correspondientes de la otra cadena. Debido a la afinidad química entre las bases, los nucleótidos que contienen adenina se acoplan siempre con los que contienen timina, y los que contienen citosina con los que contienen guanina. Las bases complementarias se unen entre sí por enlaces químicos débiles llamados enlaces de hidrógeno.
 asociación específica con los correspondientes de la otra cadena. Debido a la afinidad química entre las bases, los nucleótidos que contienen adenina se acoplan siempre con los que contienen timina, y los que contienen citosina con los que contienen guanina. Las bases complementarias se unen entre sí por enlaces químicos débiles llamados enlaces de hidrógeno.
asociación específica con los correspondientes de la otra cadena. Debido a la afinidad química entre las bases, los nucleótidos que contienen adenina se acoplan siempre con los que contienen timina, y los que contienen citosina con los que contienen guanina. Las bases complementarias se unen entre sí por enlaces químicos débiles llamados enlaces de hidrógeno.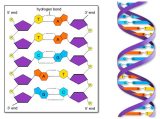 En 1953, el bioquímico estadounidense James Watson y el biofísico británico Francis Crick publicaron la primera descripción de la estructura del ADN. Su modelo adquirió tal importancia para comprender la síntesis proteica, la replicación del ADN y las mutaciones, que los científicos obtuvieron en 1962 el Premio Nobel de Medicina por su trabajo.
En 1953, el bioquímico estadounidense James Watson y el biofísico británico Francis Crick publicaron la primera descripción de la estructura del ADN. Su modelo adquirió tal importancia para comprender la síntesis proteica, la replicación del ADN y las mutaciones, que los científicos obtuvieron en 1962 el Premio Nobel de Medicina por su trabajo.
Síntesis Proteica
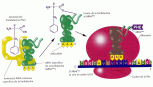 Una de las tareas más importantes de la célula es la síntesis de proteínas, moléculas que intervienen en la mayoría de las funciones celulares.
Una de las tareas más importantes de la célula es la síntesis de proteínas, moléculas que intervienen en la mayoría de las funciones celulares.
El material hereditario conocido como ácido desoxirribonucleico (ADN), que se encuentra en el núcleo de la célula, contiene la información necesaria para dirigir la fabricación de proteínas.

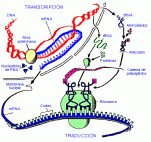 El ADN incorpora las instrucciones de producción de proteínas. Una proteína es un compuesto formado por moléculas pequeñas llamadas aminoácidos, que determinan su estructura y función.
El ADN incorpora las instrucciones de producción de proteínas. Una proteína es un compuesto formado por moléculas pequeñas llamadas aminoácidos, que determinan su estructura y función. La secuencia de aminoácidos está a su vez determinada por la secuencia de bases de los nucleótidos del ADN.
La secuencia de aminoácidos está a su vez determinada por la secuencia de bases de los nucleótidos del ADN.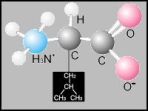 Cada secuencia de tres bases, llamada triplete, constituye una palabra del código genético o codón, que especifica unaminoácido determinado.
Cada secuencia de tres bases, llamada triplete, constituye una palabra del código genético o codón, que especifica unaminoácido determinado.
Así, el triplete GAC (guanina, adenina, citosina) es el codón correspondiente al aminoácido leucina, mientras que el CAG (citosina, adenina, guanina) corresponde al aminoácido valina.
Por tanto, una proteína formada por 100 aminoácidos queda codificada por un segmento de 300 nucleótidos de ADN.
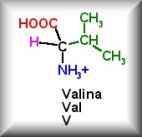 De las dos cadenas de polinucleótidos que forman una molécula de ADN, sólo una, llamada paralela, contiene la información necesaria para la producción de una secuencia de aminoácidos determinada. La otra, llamada antiparalela, ayuda a la replicación.
De las dos cadenas de polinucleótidos que forman una molécula de ADN, sólo una, llamada paralela, contiene la información necesaria para la producción de una secuencia de aminoácidos determinada. La otra, llamada antiparalela, ayuda a la replicación.
La síntesis proteica comienza con la separación de la molécula de ADN en sus dos hebras. En un proceso llamado transcripción, una parte de la hebra paralela actúa como plantilla para formar una nueva cadena que se llama ARN mensajero o ARNm.
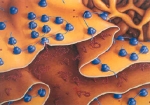
 El ARNm sale del núcleo celular y se acopla a los ribosomas, unas estructuras celulares especializadas que actúan como centro de síntesis de proteínas. Los aminoácidos son transportados hasta losribosomas por otro tipo de ARN llamado de transferencia (ARNt). Se inicia un fenómeno llamado traducción que consiste en el enlace de los aminoácidos en una secuencia determinada por el ARNm para formar una molécula de proteína.
El ARNm sale del núcleo celular y se acopla a los ribosomas, unas estructuras celulares especializadas que actúan como centro de síntesis de proteínas. Los aminoácidos son transportados hasta losribosomas por otro tipo de ARN llamado de transferencia (ARNt). Se inicia un fenómeno llamado traducción que consiste en el enlace de los aminoácidos en una secuencia determinada por el ARNm para formar una molécula de proteína.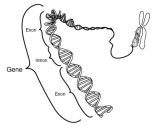 Un gen es una secuencia de nucleótidos de ADN que especifica el orden de aminoácidos de una proteína por medio de una molécula intermediaria de ARNm. La sustitución de un nucleótido de ADN por otro que contiene una base distinta hace que todas las células o virus descendientes contengan esa misma secuencia de bases alterada. Como resultado de la sustitución, también puede cambiar la secuencia de aminoácidos de la proteína resultante. Esta alteración de una molécula de ADN se llama mutación. Casi todas las mutaciones son resultado de errores durante el proceso de replicación. La exposición de una célula o un virus a las radiaciones o a determinados compuestos químicos aumenta la probabilidad de sufrir mutaciones.
Un gen es una secuencia de nucleótidos de ADN que especifica el orden de aminoácidos de una proteína por medio de una molécula intermediaria de ARNm. La sustitución de un nucleótido de ADN por otro que contiene una base distinta hace que todas las células o virus descendientes contengan esa misma secuencia de bases alterada. Como resultado de la sustitución, también puede cambiar la secuencia de aminoácidos de la proteína resultante. Esta alteración de una molécula de ADN se llama mutación. Casi todas las mutaciones son resultado de errores durante el proceso de replicación. La exposición de una célula o un virus a las radiaciones o a determinados compuestos químicos aumenta la probabilidad de sufrir mutaciones.
Funciones del ADN

-Almacenamiento de la información genética
-Replicación de su propia molécula
-Síntesis de ARN (transcripción)
-Transferencia de la información genética
La replicación o duplicación de la molécula de ADN
se produce en la interfase de la división celular, más precisamente en la fase
S, con el objetivo de conservar la información genética. Los puentes de
hidrógeno que unen las dos hileras de polinucleótidos se rompen, con lo cual
ambas cadenas se separan, sirviendo cada una de molde para fabricar una nueva
hilera complementaria. La enzima ADN polimerasa se encarga de agregar
nucleótidos fabricados por la célula que están esparcidos en el núcleo. Dicha
enzima los va añadiendo a cada hilera separada conforme con la secuencia
adenosina-timina y citosina-guanina (A-T y C-G). Al terminar la duplicación se
obtienen dos moléculas idénticas de ADN de forma helicoidal, cada una con una
hilera original y otra hilera neoformada. El núcleo tiene ahora el doble del
ADN y de proteínas que al principio. De esta manera, la información genética de
la célula madre será transmitida a las células hijas al producirse la mitosis.
ACIDO RIBONUCLEICO (ARN)

A diferencia del ADN que posee desoxirribosa y
timina, el ARN está formado por ribosa como monosacárido y uracilo como una de
las bases nitrogenadas. El ARN forma una sola cadena de polinucleótidos
dispuesta en manera lineal. Está presente en el citoplasma de las células
procariotas y eucariotas.
La formación o síntesis de ARN se realiza a partir
del ADN mediante la enzima ARN polimerasa, que copia una secuencia de
nucleótidos (genes) de una hilera del ADN.
El ARN controla las etapas intermedias en la
formación (síntesis) de proteínas.
Existen cuatro tipos de ARN con distintas funciones.
Ellos son el ARN mensajero, el ARN de transferencia, el ARN ribosómico y el ARN
heteronuclear.
-ARN mensajero (ARNm)

Se forma a partir del molde de una hilera de ADN. El
ARN mensajero transporta la información para sintetizar una proteína copiada
del ADN, desde el núcleo hasta el citoplasma, pasando por los poros de la
membrana nuclear o carioteca. Luego se acopla a los ribosomas, organelas
celulares donde se produce la síntesis de proteínas. Un codón está formado por
tres nucleótidos del ARNm. Cada codón contiene un aminoácido diferente. Por lo
tanto, a partir de la sucesión de los nucleótidos del ARNm se arma la secuencia
de aminoácidos de la proteína. Debe recordarse que una serie de aminoácidos forman
una proteína. El ARNm se degrada rápidamente por acción enzimática.
-ARN de transferencia (ARNt)

Tiene por función transportar aminoácidos hacia el
ribosoma. En un extremo de su estructura, el ARNt posee un lugar específico
para que se fije el aminoácido. En el otro extremo tiene un anticodón, formado
por tres nucleótidos que se unen al codón del ARNm por puentes de hidrógeno.
-ARN ribosómico (ARNr)

Se unen a proteínas para formar los ribosomas,
organelas formadas por dos subunidades, una mayor y otra menor. En los
ribosomas se produce la síntesis de proteínas. El ARNr se sitúa en el
citoplasma, y es el tipo de ácido ribonucleico más abundante de las células. El
ARN nucleolar, ubicado en el nucléolo de las eucariotas, es el precursor del
ARN ribosómico.
-ARN heteronuclear (ARNh)
Se aloja en el núcleo celular y su función es actuar
como precursor de los distintos tipos de ARN.
Comentarios
A. Replicación
de ADN
Gracias
a la complementación entre las bases que forman la secuencia de cada una de las
cadenas, el ADN tiene la importante propiedad de reproducirse idénticamente, lo
que permite que la información genética se transmita de una célula madre a las
células hijas y es la base de la herencia del material genético. La molécula de
ADN se abre como una cremallera por ruptura de los puentes de hidrógeno entre
las bases complementarias puntos determinados: los orígenes de replicación. Las
proteínas iniciadoras reconocen secuencias de nucleótidos específicas en esos
puntos y facilitan la fijación de otras proteínas que permitirán la separación
de las dos hebras de ADN formándose una horquilla de replicación. Un gran
número de enzimas y proteínas intervienen en el mecanismo molecular de la
replicación, formando el llamado complejo de replicación o replisoma.
B. Transcripción
de ADN A ARN
Es
donde se sintetiza un ARN usando como molde al ADN. Muchos tipos de ARN pueden
ser sintetizados así por la enzima ARN polimerasa, el ARN ribosomal el de
transferencia, los pequeños ARN nucleares o citoplasmáticos y por supuesto los
ARN mensajeros, que serán luego traducidos a una cadena polipeptídica. Luego
empieza con el ensamblaje al inicio del gen, entre los que se ensamblan están
el RNA polimerasa luego la polimerasa es liberada leyendo el gen a lo largo del
DNA. A medida que la polimerasa va desenrollando la doble hélice copia una de las
dos hebras y se crea una copia del mensaje genético los nucleótidos utilizados
entran a través de la polimerasa y se aparean con el DNA copiando las ACT y G
del gen su única diferencia es que en la copia de RNA la timina se remplazan
por unas bases estrechamente relacionadas que son los uracilos.
C. Traducción
(de ADN A proteínas)
Esto
tiene lugar en los ribosomas del citoplasma. Los aminoácidos son transportados
por el ARN de transferencia, específico para cada uno de ellos, y son llevados
hasta el ARN mensajero, dónde se aparean el codón de éste y el anti codón del
ARN de transferencia, por complementariedad de bases, y de ésta forma se sitúan
en la posición que les corresponde. Una vez finalizada la síntesis de una
proteína, el ARN mensajero queda libre y puede ser leído de nuevo. De hecho, es
muy frecuente que antes de que finalice una proteína ya está comenzando otra,
con lo cual, una misma molécula de ARN mensajero, está siendo utilizada por
varios ribosomas simultáneamente.






